Уроку предшествует знакомство с
азотом, аммиаком, солями аммония. Вместе с тем
изучением химических свойств азотной кислоты
тема «Азот и его соединения» не заканчивается.
Рекомендуется провести еще один урок по изучению
особых свойств азотной кислоты. На этом уроке
рассмотреть способность HNO3 реагировать с
металлами, стоящими в ряду напряжений металлов
до и после водорода по разным схемам, в
зависимости от активности металла и
концентрации кислоты, а также обсудить
качественную реакцию на азотную кислоту,
взаимодействие азотной кислоты с белком
(ксантопротеиновая реакция) и окисление
концентрированной азотной кислотой
органических соединений (скипидара, бензина,
целлюлозы). Такая раскладка изучаемого материала
позволит творчески работающему учителю на
следующем уроке выявить степень усвоения
данного материала. Логическим завершением темы
явится проверочная или контрольная работа по
всему изученному материалу. Тип урока. Урок усвоения новых знаний.
Форма урока. Урок-лекция.
Цели. Изучить химические свойства азотной
кислоты (реакции, протекающие в растворах).
Повторить материал о реакциях ионного обмена и
условиях их протекания до конца, опираясь на
теорию электролитической диссоциации. Развить
познавательный интерес учащихся к химической
науке. Формировать всесторонне развитую,
гармоничную личность. Закрепить навыки работы с
лабораторным оборудованием и правила проведения
лабораторного демонстрационного эксперимента.
Оборудование и реактивы. Штатив с
пробирками, асбестовые сетки, штатив для
демонстрационных пробирок, демонстрационные
пробирки или химические стаканы (10 шт.),
спиртовка, спички, пробиркодержатель; медные
опилки, оксид меди(II), растворы азотной кислоты,
хлорида железа(III), гидроксида натрия или калия,
карбоната натрия (или кусочек мрамора),
индикаторов – фенолфталеина, лакмуса и
метилового оранжевого (в специальной посуде),
нитратов калия, натрия и бария, магниевые опилки,
роданид калия или аммония, порошок сухого
горючего, дихромат аммония.
После изучения материала учащиеся должны знать:
• химические свойства азотной кислоты в свете
теории электролитической диссоциации (кроме
особых свойств);
• признаки протекания реакций ионного обмена
до конца;
• что такое электролит и каковы его отличия от
неэлектролита;
уметь:
• писать уравнения реакций с участием азотной
кислоты в молекулярном, полном и сокращенном
ионном видах;
• определять по внешним признакам, протекает
ли данная химическая реакция до конца;
• грамотно работать с лабораторным
оборудованием.
План фронтальной работы с
классом
1. Определение темы урока.
2. Выявление цели урока.
3. Изложение материала в форме лекции. |
В силу достаточно большого объема,
громоздкости материала рекомендуется по
возможности отводить на изучение темы урока 50
мин учебного времени, причем начать урок следует
не с проверки заданного к уроку домашнего
задания (если таковое было), а с определения темы
и непосредственного изложения нового материала
в лекционной форме.
ХОД УРОКА
Начинается урок с занимательной минутки –
демонстрации опытов «Вулканчик», «Бенгальские
огни» (желтый, фиолетовый и зеленый),
«Искусственная кровь». Учитель акцентирует
внимание учащихся на том, что во всех проведенных
опытах фигурируют соединения азота.
Определение цели урока проводится совместно с
учащимися по следующей логической схеме: изучены
азот N2, его бинарное соединение аммиак NH3,
соли аммония, следовательно, предстоит изучать
азотную кислоту и ее свойства. Учитель уточняет,
что будут рассмотрены свойства раствора азотной
кислоты, говорит о демонстрационном
лабораторном эксперименте, который ждет
учащихся на уроке.
Все рассматриваемые реакции азотной кислоты
записываются на доске. По ходу урока учитель
повторяет с учащимися, что реакции ионного
обмена протекают до конца, если в результате
реакции выделяется газ, образуется
малодиссоциирующее вещество вода или получается
не растворимое в воде соединение.
 Реакции
азотной кислоты Реакции
азотной кислоты
1. Азотная кислота изменяет окраску
индикаторов:
НNO3 + лакмус фиолетовый 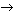 красная окраска раствора, красная окраска раствора,
НNO3 + метиловый оранжевый 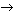 красная окраска раствора. красная окраска раствора.
В силу сложности формул индикаторов данные
взаимодействия отражают схемой, а не уравнением.
2. Взаимодействие азотной кислоты с
металлами, стоящими в ряду активности после
водорода:
Сu + 4НNO3 = Сu(NO3)2 + 2Н2О
+ 2NO2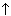 . .
Выделяющийся газ NO2 ядовит, поэтому
необходимо проводить опыт в вытяжном шкафу.
Чтобы реакция началась быстрее, раствор азотной
кислоты можно подогреть.
Уравнение реакции записывают в полном и
сокращенном ионном видах:
Сu0 + 4Н+ + 4NO3–
= Сu2+ + 2NO3– + 2Н2О + 2NO2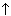
(полное ионное уравнение),
Сu0 + 4Н+ + 2NO3–
= Сu2+ + 2Н2О + 2NO2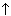
(сокращенное ионное уравнение).
Учитель напоминает правила записи уравнений
реакций в полном и сокращенном ионном видах.
В растворе на ионы не распадаются оксиды, газы,
вода, соединения, обозначенные в таблице
растворимости буквами «Н» и «М». С зарядом 0
записываются металлы и неметаллы в свободном
виде, вступающие в реакции или образующиеся в
результате химической реакции.
3. Взаимодействие азотной кислоты с
основными оксидами:
СuО + 2НNO3 = Сu(NO3)2 + 2Н2О,
СuО + 2Н+ + 2NO3– = Сu2+
+ 2NO3– + 2Н2О
(полное ионное уравнение),
СuО + 2Н+ = Сu2+ + 2Н2О
(сокращенное ионное уравнение).
4. Взаимодействие азотной кислоты с
основаниями.
Непосредственно перед опытом получают
гидроксид железа(III) по уравнению реакции:
FeCl3 + 3КОН = 3КСl + Fe(ОН)3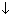 . .
Затем действием азотной кислоты растворяют
осадок Fe(OH)3:
Fe(ОН)3 + 3НNO3 = Fe(NO3)3
+ 3Н2О,
Fe(ОН)3 + 3Н+ + 3NO3–
= Fe3+ + 3NO3– + 3Н2О
(полное ионное уравнение),
Fe(ОН)3 + 3Н+ = Fe3+ + 3Н2О
(сокращенное ионное уравнение).
5. Взаимодействие азотной кислоты с солями,
образованными более слабыми и летучими
кислотами:
СаСО3 + 2НNO3 = Са(NO3)2
+ 2Н2О + СО2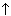 , ,
СаСО3 + 2Н+ + 2NO3–
= Са2+ + 2NO3– + 2Н2О + СО2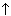
(полное ионное уравнение),
СаСО3 + 2Н+ = Са2+ + 2Н2О
+ СО2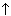
(сокращенное ионное уравнение).
Таким образом, химические свойства азотной
кислоты изучены. После этого ученики называют
три признака протекания реакций ионного обмена
до конца.
Отличившиеся на уроке получают оценки, учитель
обосновывает, почему он ставит ту или иную оценку
ученику.
Домашнее задание. По учебнику О.С.
Габриеляна «Химия-9» (М.: Просвещение, 2000) § 26;
записи в тетради. В конце урока учитель раздает
карточки с тестовыми заданиями трех уровней
сложности (на оценки «5», «4» или «3», в зависимости
от способностей учащегося и по его желанию) на
повторение уже изученного материала по теме
«Азот и его соединения». Это письменное домашнее
задание.
Если в конце урока остается время, то учащиеся
начинают работу с карточками. Первые трое,
правильно ответившие на вопросы тестов, получают
оценку «5» с занесением в журнал.
 Тестовые
задания по теме «Азот и его соединения» Тестовые
задания по теме «Азот и его соединения»
В а р и а н т 1 (на оценку «5»)
1. Азотную кислоту можно получить но схеме:
а) NO2 + O2 + H2O 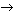 … ; … ;
б) NaNO3 + HCl 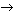 … ; … ;
в) NO + H2O 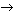 … ; … ;
г) NH3 + H2O 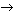 … . … .
2. При каталитическом окислении аммиака
кислородом воздуха помимо воды образуется:
а) азот; б) аммиак;
в) оксид азота(IV); г) оксид азота(II).
3. Межмолекулярная химическая связь,
возникающая между атомами водорода и атомами
сильно электроотрицательных элементов (фтора,
кислорода, азота), называется:
а) металлической; б) водородной;
в) ковалентной; г) атомной.
4. Степень окисления атома азота в катионе
аммония равна:
а) –3; б) +5; в) +3; г) 0.
5. Лабораторный способ получения аммиака:
а) Сa(OH)2 + NH4Cl 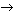 … ;
… ;
б) NH4ОН 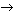 … ; … ;
в) NH4NO3 + HCl 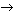 …
; …
;
г) NH4ОН + H3PO4 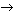 … . … .
6. Какая из солей аммония широко
используется в хлебопечении?
а) Силикат; б) сульфат; в) нитрат; г) карбонат.
7. Несолеобразующим азотсодержащем оксидом
является:
а) N2O5; б) N2O3; в) N2O; г)
NO2.
8. Разбавленная азотная кислота без
нагревания не взаимодействует с:
а) медью; б) барием; в) калием; г) литием.
9. Концентрированная азотная кислота без
нагревания не взаимодействует с:
а) калием; б) медью; в) железом; г) рубидием.
10. Составная часть ляписа:
а) нитрат серебра; б) нитрат калия;
в) нитрат алюминия; г) верного ответа нет.
В а р и а н т 2 (на оценку «4»).
1. Чилийская селитра – это:
а) нитрат бария; б) нитрат натрия;
в) нитрат кальция; г) нитрат алюминия.
2. При некаталитическом окислении аммиака
кислородом воздуха помимо воды образуется:
а) азот; б) нитрат аммония;
в) азотная кислота; г) гидразин.
3. Формула катиона аммония:
а) NH3; б) N3–; в) NH4+;
г) N2O5.
4. Валентность атома азота в катионе аммония
равна:
а) I; б) III; в) VI; г) IV.
5. Второе название хлорида аммония:
а) поташ; б) селитра; в) нашатырь; г) купорос.
6. Формула аммиачной селитры:
а) (NH4)2CO3; б) NH4Cl;
в) (NH4)3PO4; г) NH4NO3.
7. При взаимодействии оксида азота(IV) с водой
образуются:
а) азотная и азотистая кислоты;
б) аммиак и гидразин;
в) аммиак и гидразон;
г) гидроксид аммония.
8. Бурый газ (оксид азота) имеет формулу:
а) N2O3; б) NO2; в) N2O; г) NO.
9. С порошкообразной серой при нагревании
может взаимодействовать:
а) угольная кислота; б) азотная кислота;
в) соляная кислота; г) кремниевая кислота.
10. При разложении нитратов помимо прочих
продуктов выделяется:
а) азот; б) хлор; в) водород; г) кислород.
В а р и а н т 3 (на оценку «3»)
1. Степень окисления азота –3 реализуется в
соединении:
а) N2O; б) N2O4; в) Li3N; г) N2O5.
2. При обычных условиях азот реагирует
только с:
а) железом; б) оловом; в) барием; г) литием.
3. Аммонал – это смесь аммиачной селитры с
порошкообразными:
а) фосфором и кремнием;
б) алюминием и углем;
в) железом и серой;
г) медью и бором.
4. Самой сильной кислотой из приведенных
является:
а) угольная; б) сернистая;
в) азотная; г) сероводородная.
5. Реакцией ионного обмена не является
взаимодействие:
а) азота с магнием;
б) азотной кислоты с гидроксидом натрия;
в) карбоната натрия с азотной кислотой;
г) оксида калия с азотной кислотой.
6. Оксид азота(IV) выделится в качестве
продукта реакции:
а) азотной кислоты с карбонатом кальция;
б) концентрированной азотной кислоты с медью;
в) разбавленной азотной кислоты с гидроксидом
аммония;
г) азотной кислоты с оксидом магния.
7. Азотная кислота не реагирует с:
а) серой;
б) магнием;
в) оксидом алюминия;
г) угольной кислотой.
Ответы на тестовые задания
В а р и а н т 1. 1 – а, 2 – г, 3 – б, 4
– а, 5 – а, 6 – г, 7 – в, 8 – а, 9 –
в, 10 – а.
В а р и а н т 2. 1 – б, 2 – а, 3 – в, 4 –
г, 5 – в, 6 – г, 7 – а, 8 – б, 9 – б, 10
– г.
В а р и а н т 3. 1 – в, 2 – г, 3 – б, 4 –
в, 5 – а, 6 – б, 7 – г.
| 
