Цели. Закрепить представления об
особенностях состава и структуры, взаимного
влияния атомов и характерных свойств моно-, ди- и
полисахаридов на примере  -D-глюкозы, сахарозы и крахмала. -D-глюкозы, сахарозы и крахмала.
Оборудование и реактивы.
Штатив с
пробирками, стеклянная палочка, стеклянная
воронка, фильтр, водяная баня, центрифуга,
химический стакан на 50 мл (2 шт.), шпатель, железный
штатив с кольцом, санитарная склянка; NaHCO3
(кристал.), CuSO3 (кристал.), растворы глюкозы ( = 1%), крахмального
клейстера ( = 1%), крахмального
клейстера ( = 1%),
сахарозы ( = 1%),
сахарозы ( = 20% и = 20% и  = 1%), NaOH ( = 1%), NaOH ( = 10%), = 10%),
CuSO4 ( = 5%), Н2SO4
( = 5%), Н2SO4
( = 10%), [Ag(NH3)2]OH
(аммиачный р-р), Ca(OH)2 (свежеприготовленное
известковое молоко), раствор I2 в KI
(разбавленный дистиллированной водой до желтой
окраски). = 10%), [Ag(NH3)2]OH
(аммиачный р-р), Ca(OH)2 (свежеприготовленное
известковое молоко), раствор I2 в KI
(разбавленный дистиллированной водой до желтой
окраски).
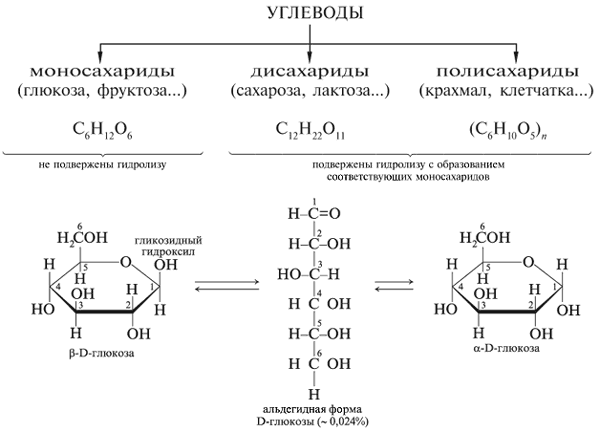
Глюкоза – альдегидоспирт, ей свойственны
реакции, характерные для многоатомных спиртов
(образование простых и сложных эфиров, окисление
и т. д.) и для альдегидов (реакция «серебряного
зеркала» с аммиачным комплексом [Ag(NH3)2]OH
и реакция с Cu(OH)2 в избытке щелочи, все на
водяной бане). Однако с фуксинсернистой кислотой
окрашивание, свойственное альдегидам,
появляется лишь при длительном стоянии
(постепенный сдвиг химического равновесия).

Существование веществ в нескольких,
находящихся в состоянии химического равновесия
изомерных формах – таутомерия (сами изомеры
– таутомеры).

Сахароза (дисахарид) не обладает
восстанавливающими свойствами, т.е. оба
гликозидных гидроксила исходных мономеров
участвуют в образовании эфирной связи и не
способны переходить в нециклическую таутомерную
форму альдегида и кетона. Это становится
возможным при гидролизе дисахарида в кислой (рН
< 7) среде на водяной бане. Сахарозе свойственны
реакции многоатомных спиртов: образование
ярко-синего сахарата меди(II) и осадка сахарата
кальция C12H22O11•3СaO•6H2O
(может быть иного состава), на чем основаны методы
очистки сахара в производстве.


Характерное для крахмала синее
окрашивание с раствором йода в йодиде калия
(разбавленном водой) в процессе гидролиза
изменяется на фиолетовое (амилодекстрины), далее
на красное (эритродекстрины), и, наконец,
возникающая желтая окраска йода уже не будет
изменяться. Образующуюся в конечном итоге
глюкозу можно обнаружить характерными
качественными реакциями.

| Порядок работы |
Задания |
Наблюдения и
выводы |
| В пробирку
налить 3–4
мл 1%-го раствора глюкозы и половинный объем 10%-го
раствора едкого натра. K смеси прибавить по
каплям (при встряхивании) 5%-й раствор медного
купороса.Смесь поместить на водяную баню,
постоянно следить за изменением цветовой гаммы |
Что происходит с
осадком образовавшегося гидроксида меди(II)? О чем
говорит изменение цвета смеси до помещения на
водяную баню? Что происходит при нагревании
смеси на водяной бане? Записать уравнения
происходящих реакций, сделать обобщающий вывод |
… |
| В чистую
пробирку
налить 3–4 мл аммиачного раствора оксида
серебра(I), добавить 2 мл 1%-го раствора глюкозы и
поместить в нагретую (70–80 °С) водяную баню.
Держать 5–10 мин, после чего осмотреть пробирку.
Жидкость из пробирки вылить в специальную
склянку |
Что собой
представляет аммиачный раствор оксида серебра(I)?
Что наблюдается на стенках пробирки по окончании
реакции? Записать уравнения реакций образования
реагента и его взаимодействия с глюкозой.
Обосновать изменения, происходящие с глюкозой |
… |
| В пробирке
(стаканчике) к 5 мл 20%-го раствора сахарозы
прибавитьпо каплям свежеприготовленное
известковое молоко (при помешивании стеклянной
палочкой). Всего прибавить 2,5 мл известкового
молока, размешать и через несколько минут смесь
отфильтровать. Фильтрат нагретьдо кипения, затем
охладить |
Убедиться, что
плохо
растворимое в воде известковое молоко
растворяется в растворе сахарозы. Пояснить
причину. При каких условиях фильтрат содержит
сахарат кальция? Что наблюдаетсяпри нагревании,
а затем при охлаждении фильтрата? Kакие
промышленные методы основанына способности
сахарозы образовывать растворимые сахараты
кальция? |
… |
K 3–4 мл 1%-го
раствора
сахарозы в пробирке прилить 0,5–1 мл 10%-го раствора
H2SO4, кипятить содержимое
1–2 мин на водяной бане. Затем 0,5 мл гидролизата
отлить в другую пробирку, а весь оставшийся
раствор при охлаждении нейтрализовать сухим NaHCO3
(добавлять небольшими порциями до прекращения
выделения газа СО2). После нейтрализации
добавить равный объем свежеприготовленного
раствора 5%-го CuSO4 в избытке 10%-го раствора
NaOH. Взболтать смеси и поместить на водяную баню,
не прекращая наблюдения. Остаток гидролизата
(0,5 мл) проверить на фруктозу реактивом
Селиванова –3 мл (0,05 г резорцина в 100 мл соляной
кислоты (1:1)) |
Что происходит с
дисахаридом – сахарозой – при нагревании в
кислой среде? Записать уравнение реакции в
структурной форме. Kакие способы доказательства
протекания гидролиза можно применить (назвать
реагенты и эффект)? Записать соответствующие
уравнения реакций применяемых методов.
Примечание. При нагревании с соляной
кислотой кетогексоза (фруктоза) превращается в
гидроксиметилфурфурол:
который с резорцином образует
соединение красного цвета (водяная баня  80 °С, 8 мин)
80 °С, 8 мин) |
… |
K 2 мл 1%-го
крахмального
клейстера прибавить равный объем 5%-го раствора
CuSO4 в избытке 10%-го раствора NaOH
(свежеприготовленного),
взболтать, нагреть на водяной бане. В колбу
поместить 40 мл 1%-го крахмального клейстера,
добавить 5–10 мл 10%-го раствора H2SO4,
нагревать на водяной бане. В пять-шесть пробирок
налить
по 2 мл разбавленного раствора йода в йодиде
калия (отметить окраску раствора). Испытание
смеси на йод продолжать через каждые 1–2 мин
нагревания на водяной бане (отбирать пробы
раствора из колбы с крахмальным клейстером и
добавлять их поочередно к раствору I2 в
пробирках). После исчезновения окраски смесь
кипятить еще 2–3 мин, после чего смесь охладить и
нейтрализовать сухим CuSO3, взбалтывая.
Профильтровать смесь и фильтрат испытать
реагентом на глюкозу |
На основании
строения
молекулы крахмала объяснить, почему при
нагревании раствора крахмала с Сu(OH)2 в
избытке щелочи наблюдается только реакция
многоатомного спирта, а реакции, характерной для
альдегидов, нет. Что происходит с крахмалом при
нагревании в кислой среде? Почему изменяется
окраска гидролизата с йодом по мере нагревания
на водяной бане? Составить схему ступенчатого
гидролиза крахмала с промежуточным образованием
декстринов, мальтозы и, наконец, глюкозы.
Подтвердить свою схему экспериментально (разная
окраска йода по мере гидролиза крахмала). Будет
ли способен соответствующий дисахарид (мальтоза)
к реакциям окисления? Ответ обосновать |
… |
Задание. Клетчатка со
смесью концентрированных кислот H2SO4
и HNO3 образует азотнокислые эфиры по
свободным гидроксигруппам [C6H7O2(OH)3]n.
Составить уравнения реакций образования
тринитрата целлюлозы (пироксилина), динитрата
(коллоксилина) и мононитрата. Указать их
практическую значимость и вычислить степень
этерификации (массовую долю  (N)) в каждом производном. (N)) в каждом производном.
|

