1. Если два элемента образуют между собой
несколько соединений, то массы одного элемента,
приходящиеся в этих соединениях на одну и ту же
массу другого элемента, соотносятся между собой
как небольшие целые числа. Такую формулировку
имеет закон:
а) кратных отношений;
б) постоянства состава;
в) эквивалентов;
г) Пруста.
2. Ученый, который ввел понятие
относительной атомной массы, – это:
а) А.Л.Лавуазье;
б) Ж.Л.Пруст;
в) Дж.Дальтон;
г) Д.И.Менделеев.
3. Атом водорода обладает минимальной
энергией, когда его электронное облако
соответствует состоянию:
а) 4s; б) 2p; в) 1s; г) 3d.
4. Энергию и размеры электронных орбиталей
определяет:
а) магнитное квантовое число;
б) орбитальное квантовое число;
в) главное квантовое число;
г) спиновое число.
5. Ориентацию орбитали в простанстве
характеризует:
а) магнитное квантовое число;
б) орбитальное квантовое число;
в) главное квантовое число;
г) спиновое число.
6. Форму атомной орбитали определяет:
а) магнитное квантовое число;
б) орбитальное квантовое число;
в) главное квантовое число;
г) спиновое число.
7. Электроны с орбитальным квантовым числом
3 получили название:
а) s-электронов;
б) p-электронов;
в) d-электронов;
г) f-электронов.
8. Электроны с орбитальным квантовым числом
1 получили название:
а) s-электронов;
б) p-электронов;
в) d-электронов;
г) f-электронов.
9. «Заполнение орбиталей одного подуровня в
основном состоянии атома начинается одиночными
электронами с одинаковыми спинами» – так
формулируется правило:
а) Хунда;
б) Паули;
в) Клечковского;
г) минимальной энергии.
10. Первый период периодической таблицы
Д.И.Менделеева состоит из:
а) одного элемента;
б) двух элементов;
в) трех элементов;
г) четырех элементов.
11. Фундаментальной основой химической
связи стала теория химического строения:
а) Б.Клапейрона;
б) Д.И.Менделеева;
в) А.М.Бутлерова;
г) А.Л.Лавуазье.
12. Выберите инертный газ, у которого на
внешней оболочке не 8 электронов:
а) гелий;
б) аргон;
в) криптон;
г) ксенон.
13. Химическая связь, образованная путем
обобществления пары электронов двумя атомами,
называется:
а) ионной связью;
б) ковалентной связью;
в) металлической связью;
г) сильно ионной связью.
14. Число ковалентных связей у атома азота
равно в ионе аммония:
а) 1; б) 2; в) 3; г) 4.
15. Идею о гибридизации атомных орбиталей
выдвинул:
а) Л.Полинг;
б) Д.И.Менделеев;
в) Ж.Б.Ламарк;
г) А.М.Бутлеров.
16. В жидкости текучесть:
а) очень высокая;
б) высокая;
в) при обычных температурах отсутствует;
г) всегда отсутствует.
17. В газах сжимаемость:
а) высокая;
б) незначительная;
в) практически отсутствует;
г) всегда отсутствует.
18. У сплавов железа в твердом веществе
плотность:
а) низкая;
б) от умеренной до большой;
в) большая;
г) умеренная.
19. «Общее давление смеси газов равно сумме
парциальных давлений компонентов» – так
формулируется закон:
а) Дальтона;
б) Пруста;
в) Менделеева;
г) Больцмана.
20. Идеальным называется газ, который
подчиняется уравнению:
а) Гесса;
б) Менделеева–Клапейрона;
в) Бутлерова;
г) Менделеева.
21. Валентные электроны у металлов:
а) не локализованы;
б) локализованы.
22. Водородная связь:
а) значительно упрочняет кристаллы;
б) разрыхляет компактную структуру кристаллов.
23. Вид атомов с одинаковым зарядом ядра –
это:
а) химическое соединение;
б) молекула;
в) химический элемент;
г) вещество.
24. Закон объемных отношений нашел
объяснение в гипотезах:
а) Авогадро;
б) Гей-Люссака;
в) Ломоносова;
г) Менделеева.
25. Спектр, излучаемый свободными атомами,
называется:
а) полосатый;
б) линейчатый.
26. Молекулярный водород имеет спектр,
имеющий название:
а) линейчатый;
б) полосатый.
27. Нагретые твердые тела дают спектр,
имеющий название:
а) линейчатый;
б) сплошной.
28. Воображаемый заряд атома элемента в
соединении, определяемый из предположения
ионного строения вещества, – это:
а) степень окисления;
б) валентность;
в) координационное число;
г) атомность.
29. Химическая связь представляет собой:
а) физическое явление;
б) биологическое явление;
в) химическое явление;
г) физико-химическое явление.
30. Разрыв связи в молекуле осуществлен
гомолитически, если образуются:
а) нейтральные атомы;
б) ионы.
31. Разрыв связи в молекуле осуществлен
гетеролитически, если образуются:
а) нейтральные атомы;
б) ионы.
32. Электрический момент диполя является
мерой:
а) полярности молекулы;
б) неустойчивости молекулы;
в) устойчивости молекулы;
г) сложности молекулы.
33. Явление смещения электрических зарядов
под действием каких-то сил – это:
а) сцинтилляция;
б) поляризация;
в) координация;
г) электросинтез.
34. Смешивание орбиталей может происходить в
отсутствие электронов на орбиталях и при наличии
спаренных электронов на одной или нескольких
орбиталях. Такое явление называется:
а) гибридизация;
б) электросинтез;
в) сцинтилляция;
г) поляризация.
35. Многоцентровая химическая связь с
дефицитом электронов в твердом или жидком
веществе, основанная на обобществлении внешних
электронов атомов, – это:
а) ковалентная неполярная связь;
б) ионная связь;
в) металлическая связь;
г) ковалентная полярная связь.
36. Укажите явление, которое свидетельствует
о волновых свойствах частиц:
а) дифракция электронов;
б) фотоэффект;
в) люминесценция;
г) линейчатый спектр излучения атома.
37. Фотохимические реакции свидетельствуют
о:
а) волновых свойствах частиц;
б) корпускулярных проявлениях электромагнитного
излучения.
38. Число вырываемых светом электронов прямо
пропорционально интенсивности света. Этот закон
установил:
а) Э.Резерфорд;
б) Н.Бор;
в) А.Г.Столетов;
г) А.Эйнштейн.
39. Красная граница фотоэффекта – это:
а) минимальная частота, начиная с которой
возможен фотоэффект;
б) минимальная частота, начиная с которой
фотоэффект невозможен;
в) максимальная частота, начиная с которой
возможен фотоэффект;
г) максимальная частота, при которой фотоэффект
уже невозможен.
40. Разновидности атомов данного
химического элемента, различающиеся по массе их
ядер, называются:
а) нуклоны;
б) атомы;
в) изотопы;
г) изобары.
41. Ядерные силы – это проявление:
а) сильного взаимодействия;
б) среднего взаимодействия;
в) слабого взаимодействия;
г) легкого взаимодействия.
42. Укажите, каким свойством не обладают
силы, связывающие нуклоны в ядре:
а) насыщением (каждый нуклон взаимодействует
только с ограниченным числом ближайших к нему
нуклонов);
б) зарядовой зависимостью (имеют электрическую
природу);
в) короткодействием (проявляются на расстояниях
между нуклонами, сравнимых по порядку величины с
размерами самих нуклонов);
г) зависимостью от ориентации спинов
взаимодействующих нуклонов.
43. Выберите пример взаимодействия, которое
не относится к электромагнитным
взаимодействиям:
а) 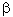 -распад; -распад;
б) кулоновское взаимодействие заряженных частиц;
в) рождение электронов и позитронов g-квантами;
г) все примеры относятся к примеру проявления
электромагнитного взаимодействия.
44. Спин электрона – это:
а) собственный момент количества движения
электрона;
б) квантовое число собственного механического
момента нуклона;
в) квантовое число собственного механического
момента позитрона;
г) квантовое число собственного
электромагнитного момента электрона.
45. Момент импульса движущегося электрона
определяется:
а) спиновым квантовым числом;
б) магнитным квантовым числом;
в) орбитальным квантовым числом;
г) главным квантовым числом.
46. Наименьшая частица вещества, обладающая
всеми его химическими свойствами, – это:
а) атом;
б) молекула;
в) позитрон;
г) нуклон.
47. Наименьшая частица химического элемента,
которая является носителем его свойств:
а) атом;
б) молекула;
в) позитрон;
г) нуклон.
48. Частично или полностью ионизированный
газ, в котором концентрации положительных и
отрицательных зарядов практически одинаковы, –
это:
а) плазма;
б) пар;
в) газ;
г) возгоняющаяся жидкость.
49. Вблизи температуры кристаллизации
многие свойства жидкостей близки к свойствам:
а) соответствующих аморфных тел;
б) соответствующих твердых тел.
50. Квантовое число m, определяющее
величину проекции момента импульса на вектор
магнитной индукции, может принимать:
а) 2l + 2 значений;
б) 3l + 2 значений;
в) 2l + 1 значений;
г) 3l + 1 значений.
Ответы на тестовые задания
1 – а; 2 – в; 3 – в; 4 – в; 5 – а; 6
– б; 7 – г; 8 – б; 9 – а; 10 – б; 11 –
в; 12 – а; 13 – б; 14 – г;
15
– а; 16 – б; 17 – а; 18 – в; 19 – а; 20
– б; 21 – а; 22 – а; 23 – в; 24 – а; 25
– б; 26 – б; 27 – б;
28
– а; 29 – г; 30 – а; 31 – б; 32 – а; 33
– б; 34 – а; 35 – в; 36 – а; 37 – б; 38
– в; 39 – а; 40 – в;
41
– а; 42 – б; 43 – а; 44 – а; 45 – в; 46
– б; 47 – а; 48 – а; 49 – б; 50 – в.
Критерии оценки (если используется в качестве учебного материала на уроке)
| Оценка |
«2» |
«3» |
«4» |
«5» |
| Выполнение работы, % |
До 48 |
50–69 |
70–91 |
92–100 |
| |
|
25–34 |
35–45 |
46–50 | | 
