1. Из приведенных ниже веществ
выберите электролит:
а) раствор сахара;
б) раствор поваренной соли;
в) бензин;
г) растительное масло.
2. Формулой моногидрата серной кислоты
является:
а) H2SO4•H2O;
б) H2SO4;
в) H2SO4•1/2 H2O;
г) H2SO4•nH2O.
3. Из приведенных ниже частиц укажите
катион:
а) К0;
б) H2;
в) S2–;
г) Na+.
4. Частица, имеющая отрицательный
заряд, называется:
а) анион;
б) катион;
в) атом;
г) молекула.
5. Литий имеет порядковый номер 3.
Укажите электронную конфигурацию атома лития:
а) 1s22s2;
б) 1s22s1;
в) 1s1;
г) 1s22s22p2.
6. Процесс распада электролита на ионы
при его растворении или расплавлении называется:
а) гидролиз;
б) гидратация;
в) диссоциация;
г) сублимация.
7. Из приведенных ниже формул солей
выберите кислую соль:
а) К2SO4;
б) (NH4)2[Fe(SO4)2];
в) (CuOH)2CO3;
г) NaH2PO4.
8. Диссоциация каких солей помимо
образования катиона металла и аниона кислотного
остатка дает еще и катион водорода? Укажите
верный вариант ответа.
а) Основных;
б) кислых;
в) средних;
г) таких солей нет.
9. Положительно заряженный электрод в
химии называют:
а) катод;
б) анод;
в) соленоид;
г) гидрат.
10. Отношение числа диссоциированных
молекул к общему числу молекул, находящихся в
растворе, для сильных электролитов близко к:
а) 1;
б) 0,5;
в) 0,25;
г) 0,1.
11. Степень диссоциации некоторого
электролита  =
0,1. Можно сказать, что этот электролит: =
0,1. Можно сказать, что этот электролит:
а) сильный;
б) средней силы;
в) слабый;
г) практически неэлектролит.
12. Реакция
Mg + H2SO4 = MgSO4 + H2
протекает до конца, т. к. выделяется:
а) вода;
б) осадок;
в) соль;
г) газ.
13. Из приведенных ниже реакций
выберите ту, которая не протекает до конца:
а) KCl + NaNO3 = ... ;
б) K2CO3 + HCl = ... ;
в) CuO + HNO3 = ... ;
г) NaOH + H2SO4 = ... .
14. Качественная реакция на хлорид-ион:
а) NaCl + H3PO4 = ... ;
б) NaCl + AgNO3 = ... ;
в) NaCl + KOH = ... ;
г) NaCl + SO2 = ... .
15. В трех пробирках находятся растворы
KOH, HCl, Na2SO4. Имеются три реактива: синий
лакмус (1), BaCl2 (2), фенолфталеин (3). Укажите
верную последовательность прибавления
реактивов 1, 2, 3 в пробирки для обнаружения
веществ в растворах. Варианты ответа:
а) 1, 3, 2;
б) 3, 1, 2;
в) 1, 2, 3;
г) 2, 3, 1.
16. В какой из приведенных ниже реакций
наблюдаются два признака, позволяющих говорить о
том, что данная реакция ионного обмена идет до
конца?
а) KCl + NaOH = ... ;
б) НCl + КOH = ... ;
в) Na2CO3 + HNO3 = ... ;
г) CaO + HNO3 = ... .
17. Реакции какого типа не бывают
окислительно-восстановительными?
а) обмена;
б) замещения;
в) разложения;
г) соединения.
18. Из приведенных ниже реакций
выберите ту, которая протекает без изменения
степени окисления:
а) H2 + O2 = ... ;
б) СuO + H2 = ... ;
в) Mg + HCl = ... ;
г) K2O + CO2 = ... .
19. В реакции
CuSO4 + Fe = FeSO4 + Cu
окислителем является:
а) Сu0;
б) Fe0;
в) Cu2+;
г) Fe2+.
20. Имеются три пробирки с растворами
веществ: NaСl, K2CO3, MgSO4. Какой цвет
приобретет фенолфталеин в каждом растворе?
Выберите верный ответ.
а) малиновый, бесцветный, бесцветный;
б) бесцветный, малиновый, бесцветный;
в) бесцветный, малиновый, малиновый;
г) бесцветный, бесцветный, малиновый.
21. Какая из солей не подвергается
гидролизу?
а) NaCl;
б) K2CO3;
в) Al2S3;
г) Na2S.
22. В растворе какой соли индикатор
метиловый оранжевый не изменяет окраску?
а) AlCl3;
б) Na2CO3;
в) K2S;
г) KCl.
Подгруппа кислорода
23. Какая из приведенных ниже
электронных конфигураций соответствует атому О
(кислород)?
а) 1s22s22p2;
б) 1s22s22p6;
в) 1s22s22p4;
г) 1s22s22p63s2.
24. Электронная конфигурация иона S2–
– это:
а) 1s22s22p63s23p6;
б) 1s22s22p63s2;
в) 1s22s22p4;
г) 1s22s22p63s23p44s2.
25. Элементы VI группы главной подгруппы
– это:
а) азот, фосфор, мышьяк, сурьма, висмут;
б) кислород, сера, селен, теллур, полоний;
в) фтор, хлор, бром, йод, астат;
г) кислород, сера, хром, селен, молибден, теллур,
вольфрам, полоний.
26. В возбужденном состоянии сера может
проявлять степень окисления +4, при этом
распределение электронов по орбиталям будет
следующим:
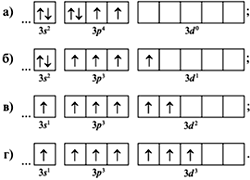
27. Число атомов в кольце
кристаллической серы равно:
а) 6;
б) 9;
в) 4;
г) 8.
28. При взаимодействии меди с
концентрированной серной кислотой помимо соли и
воды выделяется:
а) S;
б) SO2;
в) SO3;
г) H2S.
29. Какая из приведенных ниже реакций
не протекает?
а) Na + H2SO4 (конц.) = ... ;
б) Mg + H2SO4 (конц.) = ... ;
в) Pb + H2SO4 (конц.) = ... ;
г) Zn + H2SO4 (конц.) = ... .
30. Кислые соли серной кислоты
называют:
а) гидросульфаты;
б) гидросульфиды;
в) гидросульфиты;
г) сульфаты.
31. Качественная реакция на серную
кислоту:
а) H2SO4 + KOH = ... ;
б) H2SO4 + BaCl2 = ... ;
в) H2SO4 + Сu = ... ;
г) H2SO4 + Na2O = ... .
Скорость химических реакций
32. Равновесие реакции
2Н2S (г.) + 3О2 (г.) = 2Н2О (г.)
+ 2SO2 (г.)
при повышении давления смещается:
а) вправо;
б) влево;
в) давление не влияет на равновесие.
33. Вещество, ускоряющее ход реакции, но
при этом не расходующееся:
а) ингибитор;
б) катализатор;
в) индикатор.
34. Повышение температуры в реакции
2Н2 + О2 = 2Н2О + Q кДж
сказывается следующим образом:
а) не оказывает влияния;
б) смещает равновесие вправо;
в) смещает равновесие влево.
35. Не оказывает воздействия на
реакции, протекающие в твердой фазе, следующий
фактор:
а) концентрация реагентов;
б) температура;
в) природа реагирующих веществ;
г) степень измельчения реагентов.
36. Натрий энергичнее реагирует с
водой, чем железо, поскольку:
а) натрий – газообразный элемент;
б) натрий – катализатор этой реакции;
в) натрий – ингибитор этой реакции;
г) натрий – щелочной металл.
Подгруппа азота
37. Атом фосфора имеет конфигурацию:
а) 1s22s22p63s23p3;
б) 1s22s22p5;
в) 1s22s22p63s23p64s2;
г) 1s22s22p63s23p5.
38. Между атомами в молекуле азота
существует:
а) двойная связь;
б) тройная связь;
в) одинарная связь;
г) пять химических связей.
39. Азот достаточно инертен по
отношению к металлам, но сравнительно легко
протекает следующая реакция:
а) Cu + N2 = ... ;
б) Zn + N2 = ... ;
в) Al + N2 = ... ;
г) Li + N2 = ... .
40. Летучее водородное соединение
азота имеет формулу:
a) NH2;
б) N2H4;
в) NH3;
г) NО2.
41. В какой реакции азот проявляет
восстановительные свойства?
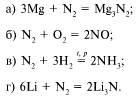
42. Вещество Mg3N2 называют:
а) нитрат магния;
б) нитрит магния;
в) сульфат магния;
г) нитрид магния.
43. Сколько свободных электронных пар
имеет азот в молекуле аммиака?
а) 2;
б) 4;
в) 1;
г) 3.
44. Аммиак в лаборатории получают по
реакции:
а) NH4Cl + Ca(OH)2 = ... ;
б) N2 + 3H2 = ... ;
в) Са3(PO4)2 + (NH4)2SO4
= ... ;
г) (NH4)3РO4 + HCl = ... .
45. Выберите ряд веществ,
соответствующий нарастанию молекулярных масс:
а) озон, аммиак, кислород;
б) аммиак, кислород, озон;
в) кислород, аммиак, озон;
г) кислород, озон, аммиак.
46. Аммиак может реагировать с соляной
кислотой по реакции
NH3 + HCl = NH4Cl.
Четвертый атом водорода присоединяется по
донорно-акцепторному механизму, при этом донором
является:
а) водород;
б) хлор;
в) азот;
г) группа 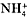 . .
47. В аммиаке и катионе аммония степень
окисления азота одинаковая: –3. Какие
валентности у атомов азота в этих соединениях?
а) Обе – III;
б) обе – IV;
в) III и II;
г) III и IV.
48. Нашатырный спирт – это:
а) NH3;
б) NH3•H2O;
в) NH4Сl;
г) N2H4.
49. Для какой реакции повышение
давления сместит равновесие вправо?
а) N2 (г.) + О2 (г.) = 2NO (г.);
б) Н2 (г.) + S (ж.) = Н2S (г.);
в) N2 (г.) + 3Н2 (г.) = 2NН3 (г.);
г) Н2 + Сl2 = 2НCl.
50. Соль PH6NO4 называется:
а) нитрат аммония;
б) фосфат аммония;
в) нитрит аммония;
г) дигидрофосфат аммония.
51. В лаборатории азотную кислоту
получают по реакции:
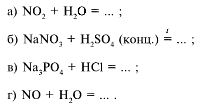
52. При взаимодействии
концентрированной азотной кислоты с серебром
помимо соли и воды выделяется газ:
а) NO2;
б) NO;
в) N2;
г) N2О.
53. При термическом разложении нитрата
калия выделяется газ:
а) N2;
б) NO2;
в) О2;
г) N2О.
54. Вещество Са3Р2
называется:
а) фосфат кальция;
б) фторид кальция;
в) фосфид кальция;
г) фосфин.
55. Чтобы получить белый фосфор нужно:
а) нагреть красный фосфор без доступа
кислорода;
б) охладить красный фосфор;
в) нагреть черный фосфор без доступа кислорода;
г) растворить красный фосфор в воде.
56. Вторая ступень диссоциации
фосфорной кислоты выражается уравнением:
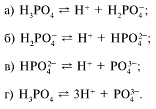
57. При каком условии протекает реакция
P2O5 + 3H2O = 2H3PO4?
а) Нагревание;
б) охлаждение;
в) измельчение Р2О5;
г) в присутствии катализатора.
58. Какая из приведенных ниже реакций
не протекает?
а) Р2О5 + КОН = ... ;
б) H3PO4 + Na2SO4 = ... ;
в) К3PO4 + AgNO3 = ... ;
г) Na3PO4 + H2SO4 (конц.) = ... .
59. Формула аммиачной селитры:
а) КNO3;
б) (NH4)3PO4;
в) NH4NO3;
г) (NH4)2SO4.
60. Микроэлемент – это:
а) цинк;
б) фосфор;
в) азот;
г) калий.
Подгруппа углерода
61. Графит является аллотропным
видоизменением:
а) кислорода;
б) углерода;
в) фосфора;
г) азота.
62. Валентность углерода в метане СН4
равна:
а) I;
б) II;
в) IV;
г) VI.
63. Каким способом нельзя получить
оксид углерода(II)?
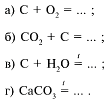
64. Соединение Al4C3
называется:
а) карбонат алюминия;
б) нитрид алюминия;
в) карбид алюминия;
г) оксид алюминия.
65. В реакции
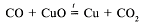
оксид углерода(II) проявляет свойства:
а) восстановительные;
б) окислительные;
в) эта реакция не идет;
г) СО является катализатором реакции.
66. Какой металл может гореть в
атмосфере СО2?
а) Медь;
б) никель;
в) магний;
г) серебро.
67. Какая реакция не протекает до конца?
а) H2O + CO2 = ... ;
б) СaO + CO2 = ... ;
в) KOH + CO2 = ... ;
г) К2СO3 + CO2 + Н2О = ... .
68. Чему равна валентность углерода в
угольной кислоте Н2СO3:
а) II;
б) IV;
в) III;
г) VI.
69. Для протекания реакции
СaСO3 = СаО + CО2
необходимым условием является:
а) охлаждение;
б) измельчение исходного СаСО3;
в) наличие катализатора;
г) нагревание.
70. Выберите ряд, соответствующий
убыванию силы кислот:
а) H2SO4, H3PO4, H2CO3;
б) H2SO4, H2CO3, H3PO4;
в) H3PO4, H2SO4, H2CO3;
г) H2СO3, H3PO4, H2SO4.
71. Какая реакция используется для
обнаружения СО2?
а) KOH + CO2 = ... ;
б) Mg + CO2 = ... ;
в) Н2О + CO2 = ... ;
г) Са(ОН)2 + CO2 = ... .
72. Кислые соли угольной кислоты
называют:
а) нитраты;
б) карбонаты;
в) гидрокарбонаты;
г) карбиды.
73. Реакция, с помощью которой нельзя
получить кремниевую кислоту:
а) H2О + SiO2 = ... ;
б) К2SiO3 + CO2 + Н2О = ... ;
в) Na2SiO3 + HCl = ... ;
г) К2SiO3 + HNO3 = ... .
74. Хрустальное стекло помимо оксидов
кальция, натрия и кремния, содержит оксиды:
а) бора;
б) свинца;
в) магния;
г) меди.
75. Формула химического стекла:
а) K2O•CaO•6SiO2;
б) Na2O•CaO•6SiO2;
в) Na2O•6SiO2;
г) СuO•Na2O•6SiO2.
*К учебнику
Ф.Г.Фельдмана, Г.Е.Рудзитиса «Химия-9».
| 
